※この時期のUpToDateにある”What’s new in family medicine”のTopicで参考にされている文献です。
―文献名―
Isla S Mackenzie, Amy Rogers, Neil R Poulter,et al.Cardiovascular outcomes in adults with hypertension with evening versus morning dosing of usual antihypertensives in the UK (TIME study): a prospective, randomised, open-label, blinded-endpoint clinical trial.Lancet.2022;400:1417-1425.
―要約-
【背景】降圧薬を夜に内服することは、朝に内服するよりも良好な転帰をもたらす可能性が研究で示唆されている。TIME(Treatment in Morning versus Evening)試験は、高血圧患者において、通常の降圧薬を夜に内服することが朝に内服することと比較して主要な心血管疾患の転帰を改善するかどうかの検討を目的とした。
【方法】TIME試験は英国で行われた前向き実用的分散型並行群間試験で、少なくとも1種類の降圧剤を服用している高血圧の成人(18歳以上)を対象に行われた。対象者は、制限、層別化、最小化なしに、通常のすべての降圧剤を朝(6:00~10:00)または夜(20:00~0:00)に服用するよう1:1で無作為に割り付けられた。複合主要評価項目は、血管死、非致死性心筋梗塞または非致死性脳卒中による入院とした。評価項目は参加者の報告またはNational Health Serviceのデータセットへの記録リンクによって同定され、治療割り付けを盲検化した委員会によって判定された。主要評価項目は、無作為に割り付けたすべての参加者からイベントが最初に発生するまでの時間として評価された。安全性は少なくとも1回の追跡調査票を提出したすべての参加者を対象に評価された。
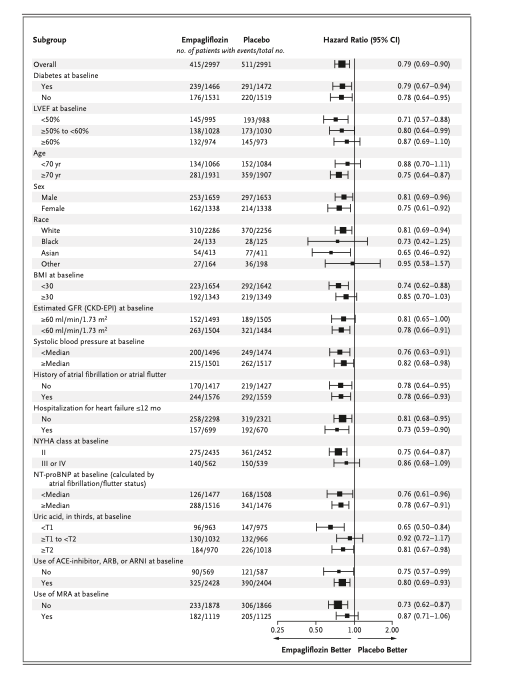
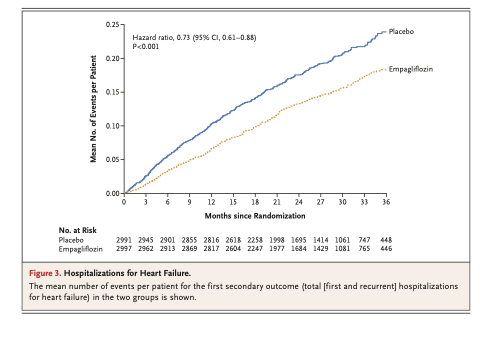
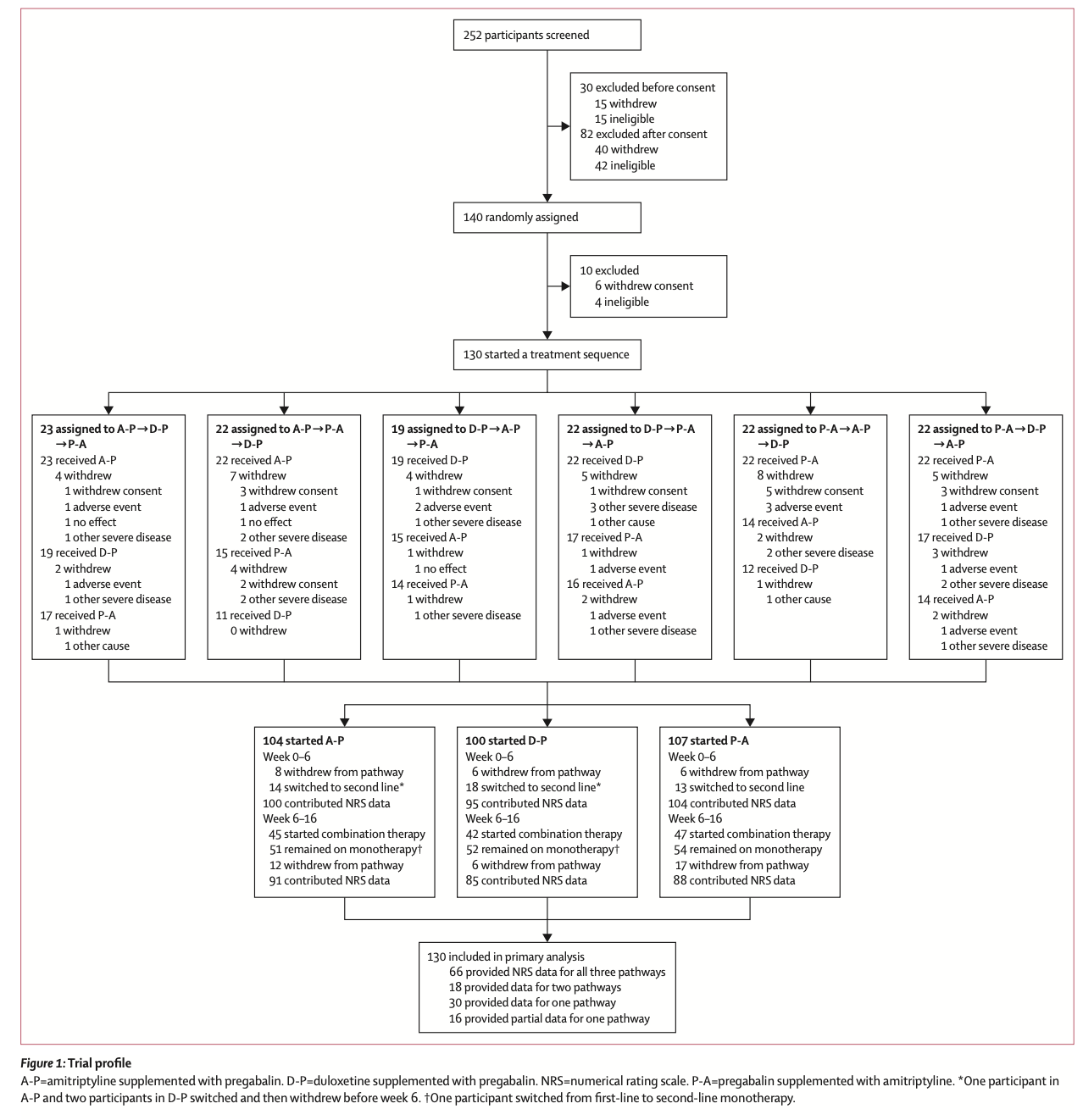
【結果】2011年12月17日から2018年6月5日の間に、24,610人がスクリーニングされ、21,104人が夜間投与群(n=10 503)または朝方投与群(n=10601)にランダムに割り付けられた。試験参加時の平均年齢は65.1歳(SD 9.3)、参加者は男性12,136人(57.5%)、女性8,968人(42.5%)、白人19,101人(90.5%)、黒人/アフリカ系/カリブ系/ブラックブリティッシュ98人(0.5%)(1,637人(7.8%)からの民族の報告なし)、そして2,725人(13.0%)に心疾患の既往がありました。試験終了時(2021年3月31日)の追跡期間中央値は5.2年(IQR 4.9~5.7)であり、夜治療に割り付けられた10,503人中529人(5.0%)、朝治療に割り付けられた10,601人中318人(3,0%)がすべての追跡調査から除外された。主要評価項目であるイベントは、夜間投与群362名(3.4%)、朝方投与群390名(3.7%)で発生した(100患者年当たり0.72イベント[95%CI 0.65-0.79]、未調整ハザード比0.95[95%CI 0.83~1.10];p=0.53 )。安全性に関する懸念は確認されなかった。
【解釈】降圧薬を夜に投与することは、朝投与と比べて、主要な心血管アウトカムに関して差がなかった。患者に適切な降圧薬を選択し、好ましくない作用を最小限に抑えた都合のよい時間に服用できるようアドバイスできます。
【discussion】すべての参加者は、割り当てられた投与時間を認識しており、このことが行動や報告に影響を与えた可能性がある。さらに、参加者が報告した有害事象は不完全であり、想起バイアスや報告バイアスの影響を受ける可能性がある。また夜間投与群では朝投与群に比べてアンケート調査からの離脱率が高かったため、群間比較において実際の有害事象発生率が過小評価された可能性があります。したがって、これらの自己報告による有害事象のデータは慎重に解釈されるべきであると考えます。そして高齢者、高血圧の家族歴がある人、高血圧治療薬の服用数が多い人、社会的剥奪度が低い人ほど家庭血圧測定に参加しやすく、一方、BMIが高い人および喫煙者は家庭血圧測定に参加しにくい傾向があることが示された。したがって家庭血圧のデータは、TIME試験の無作為化集団を必ずしも完全に代表しているわけではありません。TIME試験は、夜間高血圧やその他の日内血圧変動障害に関する試験ではなく、これらの集団における投与時間について助言するためには、さらなる研究が必要である。
【開催日】2022年12月7日(水)