※この時期のUpToDateにある”What’s new in family medicine”のTopicで参考にされている文献です。
-文献名-
Zheng NS, Annis J, Master H, Han L, Gleichauf K, Ching JH, Nasser M, Coleman P, Desine S, Ruderfer DM, Hernandez J, Schneider LD, Brittain EL. Sleep patterns and risk of chronic disease as measured by long-term monitoring with commercial wearable devices in the All of Us Research Program. Nat Med. 2024;30(9):2648. Epub 2024 Jul 19.
-要約-
Introduction
睡眠の健康は、全死亡率や、精神疾患や心血管代謝疾患などの慢性疾患と関連している。これまでの多くの研究は睡眠時間に焦点を当てており、J字型の関連が報告されており、1日の平均睡眠時間が短い(6時間以下)または長い(9時間以上)人は、さまざまな健康状態の悪化のリスクが高い。
慢性疾患と実際の睡眠パターン(睡眠の規則性や段階(N1、N2、N3、急速眼球運動(REM)など)との関連性についてはあまりわかっていない。睡眠と慢性疾患に関するほとんどの疫学研究は、自己申告の睡眠データに依存してきたが、自己申告の睡眠データでは睡眠段階を捉えることができず、長期にわたる睡眠パターンを正確に表現できない。Fitbit などの市販のウェアラブルデバイスの最近の開発により、一般の人々における睡眠パターンをポリソムノグラムと比較して優れた性能で客観的に長期にわたって測定できるようになった。これらのデバイスの人気の高まりにより、ウェアラブルデバイスから得られる指標と慢性疾患との関連性に関する大規模な疫学研究が可能になった。
この研究では、All of Us研究プログラム(AoU研究プログラム;米国国立衛生研究所が資金提供している、100万人以上の多様な人々から健康データを収集する取り組み)の縦断的な電子健康記録データと毎日の睡眠パターンを活用して、時間の経過に伴う睡眠パターンと慢性疾患の発症との関連性を調査した。
Method
我々は、消費者に表示される Fitbit由来の毎日の要約データを使用した。これには、毎日の睡眠時間、安眠できない睡眠時間 (Fitbit では、動いているが覚醒していない睡眠と定義されている)、Fitbit由来の睡眠段階 (浅い、深い、REM) が含まれる。Fitbitは、心拍数と動きに基づく独自のアルゴリズムを使用して睡眠段階を推定し、3 時間を超える睡眠期間の睡眠段階のみを推定する。アルゴリズムの検証研究に基づき、Fitbitは「浅い」睡眠をN1+N2、「深い」睡眠をN3、「REM」を急速眼球運動睡眠にマッピングしている。
発見分析では、各参加者のモニタリング期間全体にわたって毎日の睡眠パターンを平均した。Fitbitから取得した睡眠段階データが利用可能な睡眠期間のみが、毎日の睡眠段階の平均を推定するために使用された。Fitbitモニタリング期間は、参加者がFitbitアカウントを作成した時点で開始される。睡眠不規則性を、毎日の睡眠時間の標準偏差として定義した。各睡眠段階の毎日の割合 (睡眠段階の時間/総睡眠時間)を計算した。一般的な睡眠スケジュールパターンを特徴付けるために、午後8時から午前2時までと定義される「従来の」時間帯の睡眠開始の割合を計算した。この時間帯を選んだのは、コホートの平均睡眠開始時刻が午後11時10分であり、ヒートマップにプロットしたときに睡眠開始時刻の大部分がこの時間枠内にあったためである(図1)。週末は典型的な睡眠スケジュールの代表性が低いため、「伝統的な」睡眠開始時刻の分析から除外された。
Results
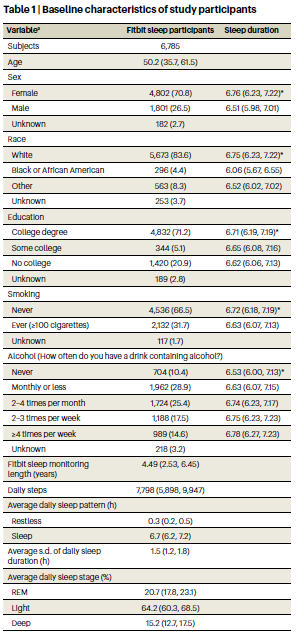
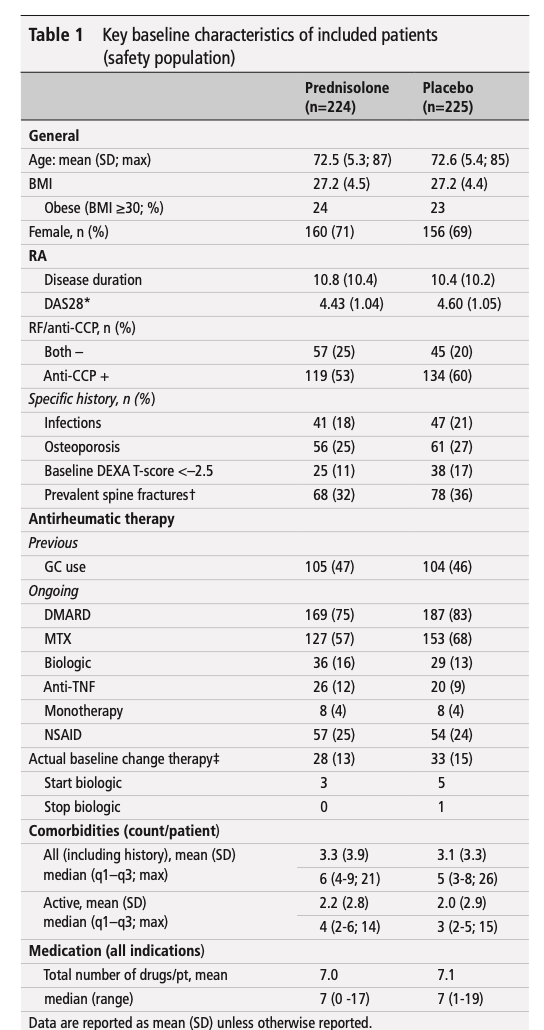
Fitbit から取得した睡眠データを持つ14,892人を特定した。電子健康記録データがリンクされ、Fitbitモニタリング期間が6か月以上で、睡眠時間が4時間未満の夜が30%未満である成人参加者6,785人が分析に含まれ、その結果6,477,023人泊となった。年齢の中央値は50.2歳(四分位範囲=35.7~61.5)であった(表1)。参加者のほとんどは女性(71%)、白人(84%)、大学教育を受けた人(71%)であった。Fitbitモニタリング期間の中央値は4.49(2.53~6.45)年で、1日の平均歩数の中央値は 7,798 (5,898 ~ 9,947) 歩/日であった。睡眠パターンの中央値は、入眠時刻が午後11時10分(午前10時30分~午前0時)、睡眠時間が6.7(6.2~7.2)時間、不眠時間が0.3(0.2~0.5)時間、睡眠不規則性(1日の平均睡眠時間の標準偏差)が1.5(1.2~1.8)時間であった。平日における「伝統的」な時間帯(午後8時から午前2時)の入眠の割合の中央値は93.5(85.2~97.3)%であった。睡眠段階については、レム睡眠、浅い睡眠、深い睡眠に費やされた割合の中央値はそれぞれ20.7(17.8~23.1)%、64.2(60.3~68.5)%、15.1(12.7~17.5)%であった。参加者の人口統計 (自己申告の性別、自己申告の人種/民族、教育) およびライフスタイル要因 (喫煙、アルコール摂取) 別に層別化すると、睡眠時間の中央値に大きな違いがあった (表1)
睡眠パターンと発症疾患の関連性
Fitbit 由来の睡眠パターンと48の有意な関連性が特定された。これには、睡眠時間に関する2つの関連性、不眠時間に関する3つの関連性、睡眠段階に関する14の関連性、睡眠不規則性に関する24の関連性、および従来型と非従来型の睡眠開始に関する5つの関連性が含まれる。不眠症と平均不眠時間、睡眠不規則性、および従来型の睡眠開始比率との関連性など、複数の睡眠パターンにわたって有意な関連性を持つ表現型がいくつか見られた。
平均1日睡眠時間が1時間長くなるごとに、病的肥満(オッズ比(OR)=0.62、95%信頼区間(CI)=0.53~0.73)および閉塞性睡眠時無呼吸(0.77、0.68~0.87)の新たな診断を受ける確率が低下した。平均1日不眠(1時間あたり)が長くなると、睡眠障害(1.58、1.32~1.89)、甲状腺機能低下症(1.42、1.21~1.68)、息切れ(1.37、1.19~1.56)のオッズが上昇した。
睡眠不規則性の増加(毎日の睡眠時間の標準偏差の1時間あたりの変化)は、さまざまな精神疾患、睡眠障害、代謝障害の発症と関連していた。睡眠不規則性の増加に関連する慢性疾患には、本態性高血圧(1.56;1.35–1.81)、高脂血症(1.39;1.20–1.61)、肥満(1.49;1.28–1.73)などがある。また、大うつ病性障害(1.75; 1.52–2.01)、不安障害(1.55; 1.35–1.78)、双極性障害(2.27; 1.65–3.11)など、いくつかの精神疾患のオッズ上昇も観察された。さらに、睡眠不規則性の増加は、胃食道逆流症(1.46;1.26–1.68)、閉塞性睡眠時無呼吸(1.43;1.22–1.67)、喘息(1.50;1.25–1.81)、片頭痛(1.60;1.31–1.95)など、睡眠を妨げる可能性のある状態と関連していた。睡眠不規則性に関する結果の大半(24 件中 23 件)は、1 日の平均睡眠時間で調整した後も依然として有意だった。
Fitbit から得られた睡眠段階を調べたところ、レム睡眠の割合が高いほど、心房細動 (OR 0.86、95% CI 0.82~0.91)、心房粗動 (0.78、0.73~0.84)、洞房結節機能不全/徐脈 (0.72、0.65~0.80) などの心拍リズムおよび心拍数異常の発生率が低下することが分かった。浅い睡眠の割合が高いほど、心房細動(1.13;1.09–1.17)、心房粗動(1.19;1.13–1.25)、洞房結節機能不全/徐脈(1.23;1.15–1.32)、鉄欠乏性貧血(1.06;1.03–1.09)のオッズが上昇した。深い睡眠の割合が高いほど、心房細動(0.87;0.81–0.93)、大うつ病性障害(0.93;0.91–0.96)、不安障害(0.94;0.91–0.97)のオッズが低くなった。
平均睡眠時間の増加は肥満リスクの低下と関連していた(ハザード比(HR)=0.90、95% CI=0.83~0.98)のに対し、睡眠不規則性の増加は肥満リスクの増加と関連していた(1.21、1.08~1.37)。レム睡眠の割合の増加は、心不全(HR 0.51、0.26~0.99)および全般性不安障害(0.80、0.69~0.92)の発症リスクの減少と関連していた。浅い睡眠の割合の増加は、心不全(2.30;1.05–5.04)、全般性不安障害(1.31;1.13–1.52)、心房細動(1.76;1.02–3.05)の発症リスクの増加と関連していた。深い睡眠の割合の増加は、心房細動(0.59;0.35–0.99)および全般性不安障害(0.84;0.72–0.98)のリスクの減少と関連していた。
平均睡眠時間と高血圧(非線形性のP=0.003)、大うつ病(P<0.001)、全般性不安障害(P<0.001)の間には、有意な非線形の J 字型関係が認められた。平均睡眠時間の中央値(6.8時間)と比較すると、平均睡眠時間が5時間の参加者は、高血圧のリスクが29%増加し(HR=1.29、95% CI =1.09~1.54)、大うつ病のリスクが64%増加し(1.64、1.27~2.12)、全般性不安障害のリスクが 46% 増加した(1.46、1.16~1.83)。平均1日睡眠時間が10時間の参加者では、高血圧のリスクが61%増加し(1.61; 1.01–2.58)、大うつ病のリスクが163%増加し(2.63;1.31~5.31)、全般性不安障害のリスクが130%増加した(2.30;1.27–4.17)
Discussion
市販のウェアラブルデバイスからの睡眠の直接測定を使用して、睡眠パターンを客観的かつ長期的に分析する、これまでで最大の研究を実施した。日々の活動 (歩数) を考慮した後でも、睡眠の量、質、規則性と重要な慢性疾患の発症との間に、臨床的かつ統計的に有意な関係が認められた。
この研究にはいくつかの限界がある。まず、研究対象者は比較的若く、大多数が女性で、白人で、大学教育を受けている。代表性の低いコミュニティや貧困地域の人々に調査結果を一般化できるかどうかは不明であり、そのため今後の研究で優先度が高い。特に、AoU研究プログラムでは、代表性の低いコミュニティから招待された参加者に Fitbit デバイスを無料で提供することで、WEAR 研究を通じて Fitbit データを持つ参加者の多様性を拡大する積極的な取り組みが行われている。とはいえ、調査結果やポリソムノグラムのデータを持つ多様な集団を使用した過去の研究によって、私たちの調査結果の多くが裏付けられている。さらに、私たちの調査結果は、2020年に30%近くに達した、市販のウェアラブルデバイスを所有する米国の一般人口の割合の増加と非常に関連している。さらに、市販のウェアラブルデバイスの所有者は一般人口よりも概して健康であるため、この研究で報告された効果サイズと睡眠の健康状態の悪さの影響は、実際には一般人口の方が強い可能性がある。第二に、私たちの分析に含まれる睡眠データは、Fitbitから報告され、Fitbitによって計算されたものとなっている。Fitbitのアルゴリズムは、多くの研究でゴールドスタンダードのポリ睡眠ポリグラムに対して評価されてきた。これらの検証研究のうち最大規模の研究では、Fitbitはポリ睡眠ポリグラムと比較して総睡眠時間や深い睡眠の推定において有意差はなかったが、レム睡眠を11.4分過小評価していた。したがって、睡眠段階の割合の潜在的な体系的な誤推定のため、私たちの調査結果は、Fitbit以外のソースからの睡眠データには一般化できない可能性がある。
睡眠モニタリング機能を備えたウェアラブルデバイスは、ますます普及している。消費者に直接報告される睡眠パターンに基づく私たちの研究結果は、睡眠をモニタリングする参加者や健康的な睡眠習慣についてカウンセリングする医療提供者にとって非常に重要なものとなるだろう。将来、患者が生成した睡眠データを日常診療の診療記録に統合することで、医療提供者は睡眠パターンの変化を病気の早期指標としてモニタリングし、個人の臨床状況やリスクプロファイルに合わせたエビデンスに基づくガイダンスを提供できるようになる。
要約すると、睡眠の量、質、規則性が不十分であることは、肥満、心房細動、高血圧、うつ病、全般性不安障害など、数多くの慢性疾患の発症率増加と関連していることがわかった。これらの調査結果が検証されれば、特に慢性疾患のリスクが高い人に対する健康的な睡眠習慣に関する最新の推奨事項の根拠となる可能性がある。さらに、私たちの研究は、科学的発見を前進させ、患者ケアを改善するために、市販のウェアラブルデバイスからのデータを電子診療記録と統合することの価値を裏付けている。
【開催日】2025年3月5日